电位测定法测定酶的催化活性:
pH 敏感的玻璃电极可以用于测定那些产生或消耗质子的反应。出于这个目的,利用反 滴定法保持pH 的恒定,所需要的酸或碱的消耗量就可以被测定。电极控制着自动滴定器, 这个概念就是BUCHER 描述的pH-stat 技术。
一个典型的例子是脂肪酶(E.C.3.1.1.3)[9001-62-1]催化活性的测定。
某脂(甘油三酯) 被该酶水解,生产的脂肪酸被NaOH 在pH-stat 的模式下反滴定中和。 甘油三酯+H2O→甘油二酯+脂肪酸 橄榄油作为底物,和含有脂肪酶的稀释样品溶液混合温育,混合物在恒定pH 下滴定。 纪录器标绘出了NaOH 的消耗量随时间的变化曲线,所得到的斜率与酶的催化活性相关。
其 他的例子如木瓜蛋白酶(E.C.3.4.22.2)[9001-73-4]的测定和葡萄糖氧化酶(glucose oxidase, E.C.1.1.3.4)[9001-37-0]的测定。
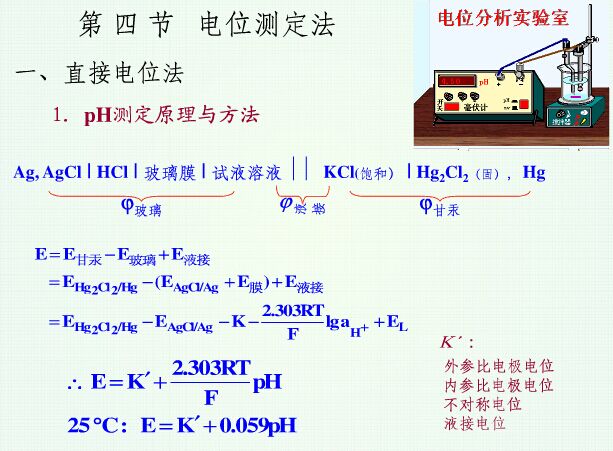
电位测定法

PH的实用定义
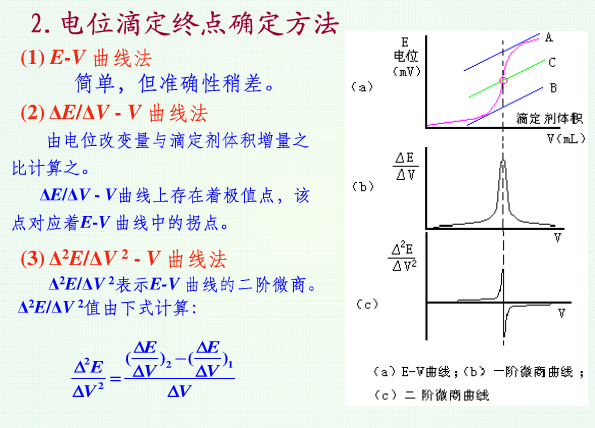
电位滴定终点确定
电位测定法的依据是待测离子的活度与其电极电位之间的关系遵守能斯特方程.
电位分析法是利用物质的电化学性质进行分析的一大类分析方法.包括直接电位法和电位滴定法.
直接电位法是利用专用电极将被测离子的活度转化为电极电位后加以测定,如用玻璃电极测定溶液中的氢离子活度,用氟离子选择性电极测定溶液中的氟离子活度[1](见离子选择性电极).
电位滴定法是利用指示电极电位的突跃来指示滴定终点.
两 种方法的区别在于:直接电位法只测定溶液中已经存在的自由离子,不破坏溶液中的平衡关系;电位滴定法测定的是被测离子的总浓度.电位滴定法可直接用于有色 和混浊溶液的滴定.在酸碱滴定中,它可以滴定不适于用指示剂的弱酸.能滴定K小于 5×10-9的弱酸.在沉淀和氧化还原滴定中,因缺少指示剂,它应用更为广泛.电位滴定法可以进行连续和自动滴定.
| 上一条: 饲料添加剂酶制剂-饲料酶制剂价格 |
| 下一条: 辐射线测定酶的催化活性 |
